MATERIAL DEL LABORATORIO
(Segundo Periodo)
Introducción:
En La presente practica esta basada al conocimiento y estudio de los materiales, y equipos en un laboratorio de química ya que el mismo no es un sitio peligroso si el experimentador es prudente y sigue todas las instrucciones con el mayor cuidado posible. Es importante no tratar de realizar experimentos por si solos, sin tener la aprobación del instructor , Las características del material dependerán de su función, ya que la manipulación de ciertos productos implica riesgos. Por ello debemos de adquirir conocimiento acerca de estos considerables elementos que durante ciertas ocasiones los usaremos y necesitaremos saber como esta compuesto y para que sirve cada uno.
OBJETIVOS :
-Familiarizarse con los materiales y equipos de laboratorio, Identificar, clasificar y establecer la utilidad de cada uno de ellos
-Identificar la clasificación de los materiales de laboratorio , definición y función
PROCEDIMIENTO :
2. Empezamos a clasificar y a describir la función de cada material de laboratorio
MARCO TEÓRICO
Los materiales de laboratorio son empleados para la comprobación experimental de las leyes y fenómenos de las ciencias naturales, estudiadas en la teoría. Para trabajar con eficiencia en el laboratorio es necesario conocer los nombres de los diferentes materiales y equipos de laboratorio.
Para clasificar la gran variedad de materiales, instrumentos y equipos se eligen dos criterios generales para su mejor estudio y son:
•Por su clase de material empleado en su fabricación.
•Por su uso especifico
- Instrumentos para medir Volúmenes Los materiales para medir volúmenes son de vidrio o de plástico transparente y están graduados. Algunos de estos materiales son:
Probeta : La probeta está formado por un tubo generalmente transparente de unos centímetros de diámetro y tiene una graduación (una serie de marcas grabadas) desde 0 ml (hasta el máximo de la probeta) indicando distintos volúmenes , La probeta es un instrumento de laboratorio volumétrico, este se usa para medir volúmenes considerables y para depositar líquidos.
-Pipeta Graduada : La pipeta graduada es un tubo de vidrio de sección uniforme, con un estrechamiento en su parte inferior. Presentan una graduación, o escala de divisiones, en 1.0 ml, 0.1 ml o 0.01 ml dependiendo de la capacidad de la pipeta. Las capacidades mas frecuentes son: 5, 10, 25 y 50 ml. Es un instrumento de vertido., Hacen posible la entrega de volúmenes fraccionados.
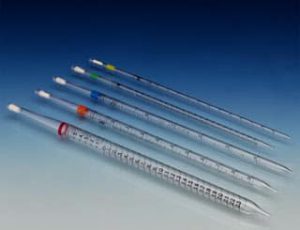
- Bureta : Las buretas son unos recipientes de forma alargada, tubulares y están graduados. Las buretas disponen de una llave de paso en su extremo inferior, esto sirve para regular el líquido que dejan salir. La bureta permite saber con gran exactitud, la cantidad de base que se ha necesitado para neutralizar un ácido, lo que permite calcular la concentración del mismo. La operación contraria, neutralizar y valorar una base con un ácido.

-Matraz aforado :Es un recipiente en forma de pera, de fondo plano y cuello alto con tapón. Es un instrumento de contenido y permite medir de forma exacta volúmenes de líquidos.En la parte del cuello presenta una marca o enrase, que indica la altura que debe alcanzar el líquido para que el matraz contenga la capacidad que indica. Los de uso mas frecuente son de capacidades 50, 100, 250, 500 y 1000 ml.
Se utilizan para preparar soluciones de concentración conocida y en la disolución de muestras en un volumen determinado.
Como todo el material de mediada exacta no debe calentarse, y en ningún caso tampoco introducir sólidos en su interior.
Se utilizan para preparar soluciones de concentración conocida y en la disolución de muestras en un volumen determinado.
Como todo el material de mediada exacta no debe calentarse, y en ningún caso tampoco introducir sólidos en su interior.

- 2. Instrumentos que se combinan SUSTANCIAS: O Utensilios para realizar mezclas
Los materiales en los que se combinan las sustancias están fabricados con Vidrio Óptico, Vidrio de Jena o Vidrio Duro. Éstos, debido a su composición, son muy resistentes a la acción de los reactivos químicos y los cambios bruscos de temperatura. Algunos nombres comerciales de estos tipos de vidrio son el Pyrex y el Kimax. Algunos ejemplos de estos materiales son:
- - Vaso de precipitados: Recipiente de vidrio o plástico. Los de vidrio son resistentes a los cambios bruscos de temperatura ,El vaso de precipitado se utiliza para mantener y calentar líquidos. Multifuncional y esencial en el laboratorio.
- Matraz Erlenmeyer : es un recipiente de forma troncocónica con una boca en la parte superior. Presenta graduación para la medida aproximada del líquido que contiene. Se utiliza para volumetrías fundamentalmente, por su facilidad para ser agitado sin derramar líquido. También se emplea para recoger líquidos provenientes de destilaciones.

•-Matraz de fondo plano : Es un frasco de vidrio, de cuello largo y cuerpo esférico. Está diseñado para calentamiento uniforme, y se produce con distintos grosores de vidrio para diferentes usos. Está hecho generalmente de vidrio borosilicatado. Se utiliza para realizar reacciones inclusive en caliente.
- Matraz de destilacion :se emplea para hervir líquidos que van a destilarse, es de forma esférica y base redonda que presenta en el cuello una tubuladura o vástago lateral, inclinado, para ser acoplado a un refrigerante.

--Matraz de dos bocas : un matraz de dos bocas se utiliza para hacer reacciones químicas en las que necesitas adicionar o controlar varios parámetros. Fundamentalmente cada boca se conecta con otro instrumental, con un termómetro, etc.
- Matraz de fondo Redondo : Es un recipiente redondo con un cuelo corto y grueso ,en la que posea una abertura.Es el recipiente utilizado para preparar soluciones.
Alli se lleva a cabo la preparacion de la solucion, y requiere de un tapon que se utiliza en el proceso en el que se prepara a solucion, para agitarlo.
- Matraz Corazón :
- En vidrio borosilicato
- Forma corazón
- 1 boca
- Esmerilado 29/32
- 250 mL de capacidad
-Matraz Kitasato : Es un matraz de vidrio que presenta un vástago. Están hechos de cristal grueso para que resista los cambios de presión. Se utiliza para efectuar filtraciones al vacío.
Utensilios de Uso especifico
- Tubo de ensayo : Es un recipiente de forma cilíndrica y fondo redondo. Se utilizan para realizar ensayos o pruebas cualitativas de reacciones con pequeñas cantidades. Existen tubos de ensayo graduados o no, con o sin tapón, de distintas capacidades y calidades: para resistir temperaturas elevadas, para centrífugas...etc
- Varilla de Agitacion ; es un instrumento de laboratorio de aproximadamente 20 cm de longitud, de forma cilíndrica, fina y maciza, utilizado en para agitar, decantar líquidos. La varilla de agitación es de vidrio.se utiliza para agitar las disoluciones con varillas huecas, mediante su calentamiento con el mechero y posterior estiramiento, se consiguen capilares
-Frasco Lavador : es un recipientes de uso común en un laboratorio. Sirven para guardar disoluciones o reactivos. Siempre deberán ir etiquetados para identificar el reactivo que contienen. Si se guarda en el una disolución que se ha preparado, además de indicar su concentración, se debe de indicar la fecha de preparación.
Existen frascos transparentes y opacos. Estos últimos se utilizan cuando el reactivo o la disolución es fotosensible.
Se presentan con tapones esmerilados, con tapones a rosca o con cuentagotas, y de distintas capacidades
-Cristalizador : Un cristalizador es un elemento perteneciente al material de vidrio que consiste en un recipiente de base ancha y poca estatura.
Su objetivo principal es cristalizar el soluto de una solución, por evaporación del solvente.
El objetivo de la forma es que tenga una base ancha es para permitir una mayor evaporación de sustancias.
- Cuentagotas : . Es un tubo hueco terminado en su parte inferior en forma cónica y cerrado por la parte superior por una perilla o dedal de goma , se usa para trasvasar pequeñas cantidades de líquido vertiéndolo gota a gota.
- Pipeta Louis Pasteur : Similar a un utensilio de gotero, generalmente formada por un tubo de vidrio con borde cónico. Sirve para hacer la transferencia de pequeñas cantidades de líquidos. Creada por el químico francés Louis Pasteur, fue nombrada en su honor.
A diferencia de otras pipetas, esta no proporciona un volumen dado. Tiene sólo abertura inferior para la entrada de líquido. En su borde superior, tiene un "globo" que, cuando se pulsa expulsa el aire. El extremo inferior se sumerge en el líquido a ser transferido y luego soltar el frasco, el líquido es aspirado en la pipeta 1
La pipeta de Pasteur se emplea cuando no se necesita una gran precisión al transferir el volumen del líquido.
-Mortero : Es un utensilio compuesto por una semiesfera hueca y un mango.
Mortero de vidrio, se utiliza para moler o pulverizar sustancias o muestras relativamente duras, antes de disolverlas o fundirlas.
Mortero de porcelana, se utiliza cuando se requiere moler o pulverizar sustancias que no son muy duras. El Mortero tiene como finalidad machacar o triturar sustancias solidas.
MATERIAL PARA PESAR :
- Balanza : Las balanzas de laboratorio son instrumentos de medición diseñados especialmente para su uso en el laboratorio, que permiten determinar el peso de un cuerpo con una división mínima de al menos 0,1 gramos. Según su tecnología podemos clasificar las balanzas de laboratorio en dos grandes grupos, balanzas de laboratorio mecánicas y electrónicas, mientras que en función de su precisión podemos clasificarlas en balanzas de precisión fina (o balanzas de precisión) y balanzas de precisión especial (o balanzas analíticas).
- Granatario : Es una aparato que permite pesar sustancias su sensibilidad es de 1 décima de gramo , La balanza granataria tiene una sensibilidad de una decima de gramo 0.01 , tiene mayor capacidad alrededor de los 2500 gr
METAL - Cucharita -Espatula : Una espátula es una herramienta que consiste en una lámina plana de metal con agarradera o mango similar a un cuchillo con punta roma , Se utiliza para tomar pequeñas cantidades de compuestos que son, básicamente, polvo. Se suele clasificar dentro del material de metal y es común encontrar en recetas técnicas el término punta de espátula para referirse a esa cantidad aproximadamente. Tienen dos curvaturas, una en cada lado, y cada una hacia el lado contrario a la otra.
- Vidrio del Reloj : Es una lámina de vidrio en forma circular cóncava-convexa. Se llama así por su parecido con el vidrio de los antiguos relojes de bolsillo. Se utiliza en química para evaporar líquidos, pesar productos sólidos o como cubierta de vasos de precipitados, y contener sustancias parcialmente corrosivas. Es de tamaño medio y muy delicado.
-Placa de Petri : es un instrumento de laboratorio el cual puede ser de cristal ode plástico, que consta de una base circular, y las paredes son de una altura baja aproximadamente de 1 cm; y una cubierta de la misma forma pero algo más grande de diámetro para que encaje como una tapa. Los hay de diferentes diámetros, los más utilizados en el laboratorio son los de 10 cm de diámetro . Se utiliza en los laboratorios principalmente para el cultivo de bacterias, mohos y otros microorganismos, soliéndose cubrir el fondo con distintos medios de cultivo (por ejemplo agar) según él microorganismo que se quiera cultivar.
-Pesasustancias : Son recipientes de vidrio que poseen una tapa esmerilada y se emplean para secar y almacenar sustancias sólidas. También existenpesasustancias de plástico, cuya principal ventaja es su robustez
METAL -Espátula : Es una lámina plana angosta que se encuentra adherida a un mango hecho de madera, plástico o metal. Es utilizada principalmente para tomar pequeñas cantidades de compuestos o sustancias sólidas, especialmente las granulares
MATERIAL PARA CALENTAR :
-Mechero Bunsen : Se utiliza para calentar, fundir o evaporar sustancias. La llama del mechero que arde correctamente es transparente y tiene un matiz azulado. No es luminosa y no desprende humo negro. En ella se distinguen con claridad dos zonas. La zona interior tiene una temperatura de 200 a 500 ºC. En su parte inferior tiene lugar la descomposición del gas y en la parte superior transcurre la combustión no completa acompañada del desprendimiento de carbono libre cuyas partículas incandescentes despiden luz.
- Mechero de Alcohol : Se utiliza cuando no se necesita un gran poder calorífico. Poseen una mecha impregnada de alcohol, que es la que arde. , Se utiliza para secado de sustancias y esterilización. Alcanza temperaturas ente 250 y 300º C
- Pinzas de Crisol : Se emplean para sujetar, colocar o retirar los crisoles y las cápsulas del horno u otra fuente de calor. Las pinzas tienen la finalidad de que la grasa de tus manos no interfiera con el análisis que estés realizando, además de que las pinzas se utilizan ya en varios casos el crisol, el vaso de precipitados y el tubo de ensayo se someten a temperaturas altas y si no ocupas las pinzas te puedes quemar o cuando te encuentras realizando una reacción exotérmica o cuando la reacción es muy violenta.
- Crisol : es una cavidad en los hornos que recibe el metal fundido. El crisol es un aparato que normalmente está hecho de grafito con cierto contenido de arcilla y que puede soportar elementos a altas temperaturas, ya sea el oro derretido o cualquier otro metal, normalmente a más de 500 °C. Algunos crisoles aguantan temperaturas que superan los 1500 °C. También se le denomina así a un recipiente de laboratorio resistente al fuego y utilizado para fundir sustancias
Metal- Rejilla de amianto : Es una rejilla metálica con una capa de amianto que es un material que soporta grandes temperaturas. La rejilla de amianto se coloca entre el fuego y el recipiente a calentar para que no entren en contacto directo e impida que se rompan debido a diferencias bruscas de temperatura.
La rejilla o malla metálica es la encargada de distribuir la temperatura de manera uniforme,
evitando que el instrumental de vidrio entre en contacto directo con la llama de mechero
y evitando que se quiebren los recipientes de vidrio por los cambios bruscos de temperatura.
La rejilla o malla metálica esta recubierta por una pequeña capa de amianto o asbesto.
evitando que el instrumental de vidrio entre en contacto directo con la llama de mechero
y evitando que se quiebren los recipientes de vidrio por los cambios bruscos de temperatura.
La rejilla o malla metálica esta recubierta por una pequeña capa de amianto o asbesto.
- Pinza Para tubo de Ensayo : Son un tipo de sujeción ajustable, generalmente de metal, que forma parte del equipamiento de laboratorio, mediante la cual se pueden sujetar diferentes objetos de vidrio (embudos de laboratorio, buretas...) o realizar montajes más elaborados (aparato de destilación). Se sujetan mediante una doble nuez a un pie o soporte de laboratorio o, en caso de montajes más complejos (línea de Schlenk), a una armadura o rejilla fija.
Las pinzas de laboratorio tienen dos partes:
Un instrumento o varilla cilíndrica, que se conecta a un soporte o rejilla mediante una doble nuez. Este acoplamiento proporciona la posibilidad de ajuste en el soporte, tanto vertical como horizontalmente.
La pinza metálica con una estructura parecida a unas tenazas. Se compone de dos brazos, que aprietan el cuello de los frascos u otros elementos de vidrio con un tornillo especial que puede ajustarse manualmente. Cada brazo posee en su cara interna un recubrimiento de PVC, corcho, fieltro o de plástico, con el fin de evitar el contacto directo del vidrio con el metal, lo que podría provocar la rotura del cristal
-Capsula de Porcelana : La capsula de porcelana es un pequeño contenedor semiesférico con un pico en su costado. Este es utilizado para evaporar el exceso de solvente en una muestra. Las Capsulas de Porcelana existen en diferentes tamaños y formas, abarcando capacidades desde los 10 ml hasta los 100 ml. , permite carbonizar sustancias y compuestos químicos, resiste elevadas temperaturas. Sirve para calentar o fundir sustancias solidas o evaporar líquidos.
- REFRIGERANTES :
-Refrigerante Recto : Es un aparato de laboratorio, construido en vidrio, que se usa para condensar los vapores que se desprenden del matraz de destilación, por medio de un líquido refrigerante que circula por éste, usualmente agua. El tubo Refrigerante está conformado por dos tubos cilíndricos concéntricos. Por el conducto interior del tubo circulara el gas que se desea condensar y por el conducto más externo circulara el líquido refrigerante.
El conducto exterior está provisto de dos conexiones que permiten acoplar mangueras de cauchos para el ingreso y posterior salida del líquido refrigerante. La entrada del líquido se efectúa por una de las conexiones.
El líquido refrigerante (generalmente agua) debe circular constantemente para generar la temperatura adecuada que permita la condensación de los vapores.
-Refrigerante de Bolas : Para condensación de vapores. Con 5 bolas (para tubos de hasta 250 mm de longitud) u 8 bolas (para tubos de 400 mm de longitud). Núcleo y conectores con esmerilado normalizado. Conexión para tubos con oliva de vidrio , Tiene Muy buena resistencia química ,Alta resistencia térmica,Mínima dilatación térmica, que proporciona alta resistencia a cambios bruscos de temperatura
- Refrigerante de Serpentín : tubo de forma frecuentemente espiral, utilizado comúnmente para enfriar vapores provenientes de la destilación en un calderín y así condensarlos en forma líquida. Suele ser de vidrio, cobre u otro material que conduzca el calor fácilmente. Este aparato se utiliza de diversas formas pero más comúnmente en el laboratorio de química.
Los serpentines se usan desde la antigüedad en la destilación de bebidas alcohólicas, aunque en la actualidad cualquier proceso de refinado de crudos u obtención de un producto químico puede utilizar un serpentín, bien para enfriar, bien para calentar líquidos o gases.
-SOPORTES

-Tripode :es un aparato de tres patas y parte superior circular o triangular, que permite estabilizar un objeto y evitar el movimiento propio de este. se utiliza cuando no se tiene el soporte universal para sostener objetos con firmeza. Es ampliamente utilizado en varios experimentos. La finalidad que cumple en el laboratorio es solo una, ya que su principal uso es como [herramienta] de sostén a fin de evitar el movimiento. Sobre la plataforma del trípode se coloca una malla metálica para que la llama no dé directamente sobre el [vidrio] y se difunda mejor el calor.
- Aro : es Instrumento metálico de laboratorio, es un soporte para ponerlo sobre un mechero bunsen, y poniéndole una placa encima, poder calentar al fuego. Generalmente se emplea como soporte para poner frascos de vidrio sobre el mechero, se puede usar anexado al soporte universal, con embudos de extracción (también llamados de decantación) . Para calentar cualquier sustancia en el laboratorio, lo sujetamos al soporte, y sobre él se coloca la rejilla, sosteniendo al recipiente que queremos calentar. Funciona sobre todo con elementos químicos calentados al fuego o mediante procesos químicos para evitar quemaduras.
- Pie : es una pieza del equipamiento de laboratorio donde se sujetan las pinzas de laboratorio, mediante dobles nueces. Sirve para sujetar tubos de ensayo, buretas, embudos de filtración, embudos de decantación, etc. También se emplea para montar aparatos de destilación y otros equipos similares más complejos.
- Gradilla para tubos de ensayo : Una gradilla es un utensilio utilizado para dar soporte a los tubos de ensayos o tubos de muestras. Normalmente es utilizado para sostener y almacenar los tubos. Este se encuentra hecho de madera, plástico o metal.
- Nuez Doble : Una doble nuez es parte del material de metal utilizado en un laboratorio de química para sujetar otros materiales, como pueden ser aros, agarraderas, pinzas, etc.
Es una pieza que posee dos agujeros con dos tornillos opuestos. Uno de los agujeros se utiliza para ajustar la doble nuez (generalmente a un soporte universal), mientras que en la otra se coloca y ajusta la pieza a sujetar.
-Pinzas para Bureta :Instrumento de metal en forma de X y sirve para sostener dos buretas en posición vertical. Para sostener una bureta se fabrican en forma de V. Estas pinzas sujetan las buretas mediante la presión de un muelle, o un tornillo. Estas pinzas deben sostenerse en un soporte universal.
-Triangulo para Crisol : Constituido por tres tubos de arcilla refractaria a base de silimanita, unidos en forma de triángulo mediante gruesos alambres de metal galvanizado.Se utiliza para sostener otros materiales como matraces, o vasos de precipitado al calentarlos. Permite trabajar con crisoles de porcelana a altas temperaturas, en procesos como el de fundir oro, ya que lo que el triangulo hace es servir de sostén para poder sostener la capsula
.Constituido por tres tubos de arcilla refractaria a base de ruesos alambres de metal galvanizado
-EMBUDOS :
-Embudo : Un embudo es una pieza cónica de vidrio o plástico que se utiliza para el trasvasijado de productos químicos desde un recipiente a otro. También es utilizado para realizar filtraciones , El embudo tiene una forma de dos conos generalmente, en su parte superior el cono mayor es el encargado de recibir la entrada de loslíquidos y el inferior es el encargado de canalizar a un recipiente el flujo proveniente de la parte superior, algunas veces la parte inferior es un cilindro. Los embudos suelen hacerse de plástico, vidrio, y otros materiales
- Embudo buchner : s una pieza del material de laboratorio de química utilizado para realizar filtraciones. Al vacío o filtración a presión asistida Tradicionalmente se produce en porcelana, por lo que se lo clasifica entre el material de porcelana. Pero también está fabricado en porcelana e incluyen una placa de vidrio sinterizado o una base de porcelana perforada. Estos se utilizan en la filtración a baja presión con un matraz de Büchner o kitasato, conectados a una bomba de vacío.
- Embudo de Seguridad : permiten un vertido de líquidos peligrosos sin ningún peligro. Sin derrames. Están fabricados en teflón de alta calidad, resistente a ácidos y disolventes. Para cualquier tamaño de boca de cualquier contenedor. Incluyen tamiz para eliminar agitadores y partículas macroscópicas. Los modelos en negro son conductores de electricidad para poder conectarlos a tierra para reducir el riesgo de incendio por electricidad estática. Compuestos por un tamiz, una dispositivo anti-salpicadura, una rosca de giro libre para mayor comodidad y un tubo de seguridad. También sirven para evitar reabsorciones o para prevenir grandes desprendimientos de gases, que puedan provocar explosiones en los aparatos.
- Embudo de Decantación : es un elemento de vidrio que se puede encontrar en los laboratorios, y que se emplea para separar dos líquidos inmiscibles. En la parte superior presenta una embocadura taponable por la que se procede a cargar su interior. En la parte inferior posee un grifo de cierre o llave de paso que permite regular o cortar el flujo de líquido a través del tubo que posee en su extremo más bajo . se utiliza principalmente para separar líquidos inmiscibles, o insolubles (no se mezclan) que se separan, por diferencia de densidades y propiedades moleculares que estos líquidos poseen. La cual mediante un tiempo se apartan en dos o más fracciones dependiendo de la cantidad de productos contenidos al interior del recipiente.
-- OTRO MATERIAL

- Frasco lavado de Gases : Son frascos cerrados con un tapón atravesado por dos tubos. Por uno de ellos se sopla, saliendo el agua por el otro. Se utilizan para enjuagar el material de laboratorio, ya sea para disolver o para lavar. se utilizan para el lavado de gases. Para ello, el frasco lavador se conecta a un flujo de gas y, en función de la aplicación, se llena con líquido. El gas se introduce en el líquido a través de un tubo, mediante lo cual se eliminan las impurezas contenidas en el gas. Mediante la selección adecuada de la solución utilizada, también es posible una humidificación (con agua), un secado (con ácido sulfúrico concentrado), e incluso una separación selectiva. El gas limpiado se extrae del frasco lavador a través de un segundo tubo.
-Columna Cromotografica :
- Las cromatografías son un grupo de técnicas de separación selectiva de moléculas, en las que los componentes de una mezcla compleja de componentes pueden ser identificados y/o purificados , Separar los componentes de la mezcla, para obtenerlos más puros y que puedan ser usados posteriormente (etapa final de muchas síntesis).
-Trompa de Agua : Es un compresor de aire que usa la fuerza del agua ,La trompa de agua es un instrumento que sirve para practicar el vacío en un recipiente. Consiste en un tubo de vidrio abierto al exterior por donde se realiza la alimentación con agua desde el exterior , el cual se va estrechando, de manera que en su parte más estrecha termina bruscamente aunque comunica con otro que, penetrando en su interior, deja un cierto hueco por el que se producirá la extracción de aire.
-kjeldahl : Son equipos utilizados para la determinación de proteínas, también se engloban en a categoría de medios por digestión de humedad y el contenido de nitrógeno por medio del método de Kjeldahl.
- Soxhlet :Es un tipo de material de vidrio utilizado para la extracción de compuestos, generalmente de naturaleza lipídica, contenidos en un sólido, a través de un disolvente afín, El soxhlet es un aparato de extracción continua para materias sólidas , Su funcionamiento consiste en hacer hervir en le matraz el disolvente con el cual se va a extraer la materia sólida deseada que se encuentra en la muestra depositado en el cartucho del “soxhlet”.
- Tubo en U : Es un tubo cilíndrico en forma de "U" de unos 2 cm de diámetro que se utiliza fundamentalmente para verificar reacciones de Oxidación‑Reducción (REDOX) donde cada una de las semirreacciones tiene lugar en cada una de las ramas , El tubo en U funciona como deposito a través del cual se transmite la presión.

- Tubo Thiele : El Tubo de Thiele se utiliza principalmente en la determinación del punto de fusión de una determinada sustancia. Para esto se llena de un líquido con un punto de fusión elevado, y se calienta. Su peculiar forma hace que las corrientes de convección formadas por el calentamiento, mantengan todo el tubo a temperatura constante.

-Desecador :es un instrumento de laboratorio que se utiliza para mantener limpia y deshidratada una sustancia por medio del vacío.Está fabricado con un vidrio muy grueso y en él se distinguen dos cavidades, la primera cavidad más grande y superior, permite poner a secar la sustancia, y la otra cavidad inferior se usa para poner el desecante, más comúnmente gel de sílice.

Introducción :
Para iniciar el estudio de la nomenclatura es necesario distinguir primero entre compuestos orgánicos e inorgánicos. Los compuestos orgánicos son los que contienen carbono, comúnmente enlazados con hidrógeno, oxígeno, boro, nitrógeno, azufre y algunos alógenos. El resto de los compuestos se clasifican como compuestos inorgánicos.
•Los compuestos inorgánicos se clasifican según la función química que contengan y por el número de elementos químicos que los forman, con reglas de nomenclatura particulares para cada grupo. Una función química es la tendencia de una sustancia a reaccionar de manera semejante en presencia de otra.
Por ejemplo, los compuestos ácidos tienen propiedades características de la función ácido, debido a que todos ellos tienen el ion hidrógeno H+1; y las bases tienen propiedades características de este grupo debido al ion OH-1 presente en estas moléculas. Las principales funciones químicas son: óxidos, bases, ácidos y sales.
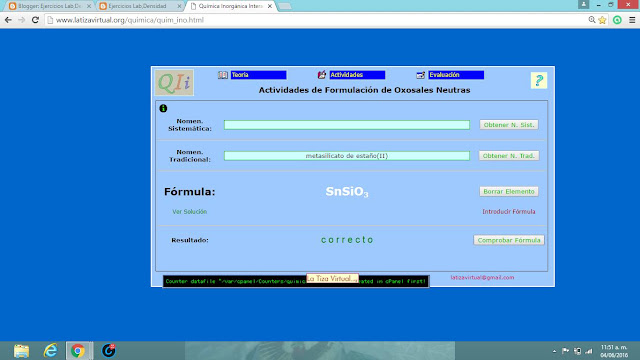
1. Entramos a la Pagina http://www.latizavirtual.org/quimica/quim_ino.html
2. Revisamos las teorías de las Nomenglaturas : Óxidos , Oxoacidos , Hidracidos
3. Damos click a actividades y Realizamos Los Problemas de cada nomenclatura según la información ya leida
4. Verificamos cada proceso y hacemos su debida corrección
- Teorias :
TEORIA NOMENGLATURA OXIDOS
ÓXIDOS
Se define un óxido como la combinación binaria de un elemento con el oxígeno. Con el oxígeno, es corriente que los elementos presenten varios grados de valencia o numero de oxidación, mientras que el O2= siempre es equivalente excepto en los peróxidos donde actúa con una valencia de -1. Para saber la valencia o valencias de un elemento cualquiera con O2 y poder formular el correspondiente óxido, basta con observar su ubicación en la tabla periódica, en la cual el número de la columna indica la valencia más elevada que presenta un elemento para con el O. Los óxidos se dividen en dos categorías según sea el tipo del elemento que se combina con el oxígeno .
ÓXIDOS BÁSICOS ( Combinación del oxígeno con elementos metálicos)
Las combinaciones del oxígeno con los metales, se llaman óxidos básicos o simplemente óxidos. El método tradicional para nombrar los óxidos básicos consiste en usar el nombre óxido de seguido de nombre del metal
EJEMPLO:
Li2O = óxido de litio
|
CaO = óxido de calcio
|
Cuando un metal presenta dos números de oxidación diferentes, para designar el óxido se emplean las terminaciones oso ( para el elemento de menor numero de oxidación) eico ( para el de mayor numero de oxidación)
EJEMPLO:
CoO = óxidocobaltoso
|
Co2O3 = óxido cobaltico
|
Para este caso, en el sistema moderno de nomenclatura, recomendado por la IUPAC, el número de oxidación del metal que se combina con el oxígeno se indica con números romanos entre paréntesis agregado al final del nombre del elemento en español:
EJEMPLO:
Co2O = óxido de cobalto ( II)
|
Co2O3 = óxido de cobalto ( III)
|
ÓXIDOS ÁCIDOS ( Combinación del oxigeno con elementos no metálicos)
Las combinaciones del oxígeno con los elementos no metálicos se llaman óxidos ácidos o anhidros ácidos
SiO2
|
=
|
dióxido de silicio
|
SeO2
|
=
|
dióxido de selenio
|
NOMENGLATURA TRADICIONAL :
| - Cuando el elemento tiene un solo estado de oxidación: |
| La nomenclatura tradicional toma en cuenta los estados de oxidación de los elementos. |
| Se nombra: "OXIDO" + nombre del elemento. Ejemplos: CaO = Oxido de Calcio Sabiendo que Ca tiene como estado de oxidación 2 y O tiene -2 |
| - Cuando el elemento tiene dos estados de oxidación: |
| * Si se toma el estado de oxidación menor: Se nombra: "OXIDO" + raiz del elemento + sufijo "OSO" Ejm: Bi2O3 = Oxido Bismutoso Sabiendo que Bi tiene como estado de oxidación 3 y O tiene -2 * Si se toma el estado de oxidación mayor: Se mombra: "OXIDO" + raiz del elemento + sufijo "ICO" Ejm: Bi2O5 = Oxido Bismutico Sabiendo que Bi tiene como estado de oxidación 5 y O tiene -2 |
| - Cuando el elemento tiene tres estados de oxidación: |
| * Si se toma el estado de oxidación menor: Se nombra: "OXIDO" + prefijo "HIPO" + raiz del elemento + sufijo "OSO" Ejm: P2O3 = Oxido hipofosforoso Sabiendo que P tiene como estado de oxidación 3 y O tiene -2 * Si se toma el estado de oxidación intermedio: Se nombra: "OXIDO" + raiz del elemento + sufijo "OSO" Ejm: PO2 = Oxido fosforoso Sabiendo que P tiene como estado de oxidación 4 y O tiene -2 * Si se toma el estado de oxidación menor: Se nombra "OXIDO" + raiz del elemento + sufijo "ICO" Ejm: P2O5 = Oxido fosforico Sabiendo que P tiene como estado de oxidación 5 y O tiene -2 |
| - Cuando tiene cuatro estados de oxidación: |
| * Si se toma el estado de oxidación menor: Se nombra: "OXIDO" + prefijo "HIPO" + raiz del elemento + sufijo "OSO" Ejm: Cl2O = Oxido hipocloroso Sabiendo que Cl tiene como estado de oxidación 1 y O tiene -2 * Si se toma el estado de oxidación intermedio menor: Se nombra: "OXIDO" + raiz del elemento + sufijo "OSO" Ejm: Cl2O3 = Oxido cloroso Sabiendo que Cl tiene como estados de oxidación 3 y O tiene -2 * Si se toma el estado de oxidación intermedio mayor: Se nombra: "OXIDO" + raiz del elemento + sufijo "ICO" Ejm: Cl2O5 = Oxido clorico Sabiendo que Cl tiene como estado de oxidación 5 y O tiene -2 * Si se toma el estado de oxidación mayor: Se nombra: "OXIDO" + prefijo "PER" + raiz del elemento + sufijo "ICO" Ejm: Cl2O7 = Oxido perclorico Sabiendo que Cl tiene como estado de oxidación 7 y O tiene -2 |
| NoMeNcLaTuRa SiStEmAtIcA |
| La nomenclatura sistematica toma en cuenta el número de moleculas de cada elemento. |
| Se nombra: Prefijo + "OXIDO DE" + prefijo + nombre del elemento. El prefijo depende del número de moleculas que tenga el elemento: 1 - mono 2 - di 3 - tri 4 - tetra 5 - penta 6 - sexta 7 - hecta 8 - octa 9 - nona 10 - deca Ejm: N2O3 = Trioxido de dinitrogeno S2O4 = Tetraoxido de diazufre Li2O = Oxido de dilitio Se2O4 = Tetraoxido de diselenio Al2O3 = Trioxido de dialuminio |
| NoMeNcLaTuRa StOcK |
| La nomenclatura stock toma en cuenta los estados de oxidación de los elementos sin contar el oxigeno. |
| Se nombra: "OXIDO DE" + nombre del elemento + (estado de oxidación del elemento) Ejm: CO2 = Oxido de carbono (IV) Sabiendo que C tiene como estado de oxidación 4 CaO = Oxido de calcio (II) Sabiendo que Ca tiene como estado de oxidación 2 Bi2O5 = Oxido de bismuto (V) Sabiendo que Bi tiene como estado de oxidación 5 Rb2O = Oxido de rubidio (I) Sabiendo que Rb tiene como estado de oxidación 1 PROBLEMAS NOMENGLATURTURA OXIDOS |
NOMENGLATURA HIDRACIDOS :
un ácido hidrácido o sencillamente hidrácido es un ácido que no contiene oxígeno, es un compuesto binario formado por hidrógeno (H), un elemento no-metálico(X) ya sea un halógeno o un anfígeno.
Nomenclatura:
La nomenclatura de los hidrácidos diferencia las sustancias gaseosas de sus soluciones ácidas.
En el caso del fluoruro de hidrógeno (ácido fluorhídrico) la molécula se suele representar como HF. Sin embargo realmente la estructura atómica de esta molécula responde a dos átomos de cada elemento H2F2.
En la nomenclatura química se escribe el ácido (HX) y después se indica que está en disolución acuosa (aq) o (ac) porque de lo contrario se generaría confusión entre las sustancias binarias, covalentes, y los ácidos.
Ejemplos:
•HF (aq) (Ácido fluorhídrico)
•HBr (aq) (Ácido bromhídrico)
•HI (aq) (Ácido yodhídrico)
•HCl (aq) (Ácido clorhídrico)
•H2S (aq) (Ácido sulfhídrico)
•H2Se (aq) (Ácido selenhídrico)
•H2Te (aq) (Ácido telurhídrico)
•El ácido cianhídrico (HCN) produce el anión cianuro (CN-).
El ácido sulfhídrico produce el anión sulfuro (S2-) y el anión ácido hidrogenosulfuro o bisulfuro (HS-). Si estos ácidos no se encontrasen en disolución acuosa se les denominaría con la nomenclatura normal para los haluros: fluoruro de hidrógeno, bromuro de hidrógeno, yoduro de hidrógeno, cloruro de hidrógeno, sulfuro de hidrógeno, seleniuro de hidrógeno, telururo de hidrógeno.
PROBLEMAS NOMENGLATURA HIDRACIDOS:
NOMENGLATURA OXOACIDOS :
Los ácidos oxácidos son compuestos ternarios formados por un óxido no metálico y una molécula de agua (H2O).
Su fórmula responde al patrón HaAbOc, donde A es un no metal o metal de transición.
Ejemplos:
- Ácido sulfúrico (H2SO4). Formado por la combinación de una molécula de H2O con una molécula de óxido sulfúrico SO3:
- SO3 + H2O → H2SO4
- Ácido sulfuroso (H2SO3). Formado por la combinación de una molécula de H2O con una molécula de óxido sulfuroso SO2:
- SO2 + H2O → H2SO3
- Ácido hiposulfuroso (H2SO2). Formado por la combinación de una molécula de H2O con una molécula de óxido hiposulfuroso SO:
- SO + H2O → H2SO2
- Ácido carbónico: CO2 + H2O → H2CO3
PROBLEMAS NOMENGLATURA OXOACIDOS:





Oxosales :
Son compuestos iónicos cuyos aniones corresponden al residuo halogénico de un oxácido. El catión, generalmente proviene de un elemento metálico cuyo número de carga z es igual a su valencia. Ejemplos,
Na3PO4 constituido por los iones Na+ y PO4 3-
CuSO4 constituido por los iones Cu2+ y SO4 2-
Al2(SO4)3 constituido por los iones Al3+ y SO4 2-
AgNO3 constituido por los iones Ag+ y NO3 -1
Para hallar los subíndices estequiométricos del catión y del anión de la fórmula química de la oxosal se procede con la misma metodología indicada para las valencias en las sales de hidrácidos, tomando a los números de carga de los iones involucrados como sus respectivas valencias.
El nombre del anión (residuo halogénico) se obtiene del nombre del ácido, simplemente cambiando los sufijos -oso por -ito, e -ico por -ato.
Na3PO4 constituido por los iones Na+ y PO4 (ANIÓN FOSFATO)-3
CuSO4 constituido por los iones Cu2+ y SO4 (ANIÓN SULFATO)-2
Al2(SO4)3 constituido por los iones Al3+ y SO4 (ANIÓN SULFATO)-2
AgNO3 constituido por los iones Ag+ y NO3 (ANIÓN NITRATO)-1
La nomenclatura química, es el conjunto de reglas o fórmulas que se utilizan para nombrar todos los elementos y compuestos químicos.
Las oxosales son compuestos, formados por un catión y el anión proviene de un ácido.
Oxoácido / Oxosal
- oso / - ito
- ico / - ato
FORMULACIÓN
SALES :
Las sales binarias son combinaciones de 2 elementos distintos del hidrógeno y del oxígeno. La unión de un elemento metálico con un elemento no metálico forman una sal neutra, mientras que la unión de un elemento no metálico con otro elemento no metálico forman una sal volátil.
Los tipos de sales neutras que existen son: fluoruros, cloruros, bromuros, yoduros, astaturos, sulfuros, telururos, seleniuros, nitruros, fosfuros, arseniuros, antimoniuros, boruros, carburos y siliciuros.
Formulación de las sales neutras
La formulación de las sales neutras siguen el siguiente modelo: MaNb, donde M: elemento metálico, N: elemento no metálico, a: valencia del elemento no metálico y b: valencia del elemento metálico.
Hay que tener en cuenta que el elemento no metálico siempre actua con la valencia fija, y esta valencia será con la que actúa frente al hidrógeno. Por lo tanto los elementos no metálicos tendrán las siguientes valencias:
F-1, Cl-1, Br-1, I-1, At-1, S-2, Te-2, Se-2, N-3, P-3, As-3, Sb-3, B-3, C-4, Si-4
Nomenclatura de las sales neutras
Las sales neutras se nombran mediante la nomenclatura tradicional, nomenclatura sistemática y la nomenclatura de stock.
Nomenclatura tradicional: la nomenclatura tradicional de las sales neutras se realiza nombrando el elemento no metálico terminado en uro seguido del elemento metálico. Para ello se debe de tener en cuenta la valencia del elemento metálico siguiendo los siguientes criterios:
- Una valencia: ...uro ...ico
- Li+1 + F-1 » LiF: fluoruro lítico
- Dos valencias:
- Menor valencia: ...uro ...oso
- Ni+2 + F-1 » NiF2: fluoruro niqueloso
- Mayor valencia: ...uro ...ico
- Ni+3 + F-1 » NiF3: fluoruro niquélico
- Menor valencia: ...uro ...oso
- Tres valencias:
- Menor valencia: ...uro hipo...oso
- Ti+2 + F-1 » TiF2: fluoruro hipotitanioso
- Valencia intermedia: ...uro ...oso
- Ti+3 + F-1 » TiF3: fluoruro titanioso
- Mayor valencia: ...uro ...ico
- Ti+4 + F-1 » TiF4: fluoruro titánico
- Menor valencia: ...uro hipo...oso
- Cuatro valencias:
- Primera valencia (baja): ...uro hipo...oso
- U+3 + F-1 » UF3: fluoruro hipouranioso
- Segunda valencia: ...uro ...oso
- U+4 + F-1 » UF4: fluoruro uranioso
- Tercera valencia: ...uro ...ico
- U+5 + F-1 » UF5: fluoruro uránico
- Cuarta valencia (alta): ...uro per...ico
- U+6 + F-1 » UF6: fluoruro peruránico
- Primera valencia (baja): ...uro hipo...oso
Nomenclatura de stock: la nomenclatura de stock de las sales binarias se comienza nombrando la raíz del elemento no metálico terminado en uro seguido por la valencia en números romanos entre paréntesis y seguido del elemento metálico junto al prefijo correspondiente a su valencia.
Ejemplos:
Au2S: sulfuro de oro (I)
FeBr3: bromuro de hierro (III)
FeBr3: bromuro de hierro (III)
Cuando el elemento metálico sólo tenga una valencia no hace falta indicar con números romanos la valencia del elemento.
Ejemplo:
CaF2: fluoruro de calcio, en lugar de fluoruro de calcio (II).
Nomenclatura sistemática: en esta nomenclatura se indica mediante un prefijo el número de átomos del elemento no metálico segido del elemento no metálico terminado en uro todo ello seguido del elemento metálico con su prefijo correspondiente.
Los prefijos utilizados que indican el número de átomos en esta nomenclatura son:
- 1 átomo: Mono
- 2 átomos: Di
- 3 átomos: Tri
- 4 átomos: Tetra
- 5 átomos: Penta
- 6 átomos: Hexa
- 7 átomos: Hepta
Ejemplos:
Au2S: monosulfuro de dioro
Au2S3: trisulfuro de dioro
Au2S3: trisulfuro de dioro
Cuando el elemento metálico sólo presenta un átomo, no se indica el prefijo mono
Ejemplos:
CaF2: difluoruro de calcio, en lugar de difluoruro de monocalcio
FeBr3: tribromuro de hierro, en lugar de tribromuro de monohierro.
FeBr3: tribromuro de hierro, en lugar de tribromuro de monohierro.
A) binarias o hidrosales
Su fórmula general es MxNy (M es un metal y N es un no metal)
Los nombres de estas sales se construye nombrando el no metal terminado en –uro .
Ejemplos:
NaF2: difluoruro de sodio; fluoruro de sodio; fluoruro sódico o de sodio
FeCl2 : dicloruro de hierro: cloruro de hierro(II); cloruro férrico
CoS: monosulfuro de cobalto; sulfuro de cobalto(II); sulfuro cobaltoso
B) Sales de oxoácidos u oxosales
Se trata de compuestos ternarios que se obtienen a partir de la reacción de oxácidos con hidróxidos.
B1) Sales neutras
Fórmula general: Mx (NyOc)n Cuando n = 1 no se escribe el paréntesis.
Ejemplos:
Fe4(P2O7)2; Tris [heptaoxodifosfato(V)] de tetrahierro(II); Pirofosfato (V) de hierro (II);
pirofosfato ferroso
Al2(SO3)3: Tris [trioxosulfato(IV)] de dialuminio; Sulfato (IV) de aluminio; sulfito de aluminio o alumínico
B2) Sales ácidas
Su fórmula general es : Mx (HyNzOw)n Si n=1 no se escribe el paréntesis.
Ejemplos
NaHSO4: hidrógenotetraoxosulfato(VI) de sodio (I); bisulfato o sulfato monoácido de sodio (o sódico)
Fe(HCO3)3: Bis[hidrógenotrioxocarbonato(IV)] de hierro (III); Hidrógeno carbonato (IV) de hierro (III): Bicarbonato férrico
Su fórmula general es MxNy (M es un metal y N es un no metal)
Los nombres de estas sales se construye nombrando el no metal terminado en –uro .
Ejemplos:
NaF2: difluoruro de sodio; fluoruro de sodio; fluoruro sódico o de sodio
FeCl2 : dicloruro de hierro: cloruro de hierro(II); cloruro férrico
CoS: monosulfuro de cobalto; sulfuro de cobalto(II); sulfuro cobaltoso
B) Sales de oxoácidos u oxosales
Se trata de compuestos ternarios que se obtienen a partir de la reacción de oxácidos con hidróxidos.
B1) Sales neutras
Fórmula general: Mx (NyOc)n Cuando n = 1 no se escribe el paréntesis.
Ejemplos:
Fe4(P2O7)2; Tris [heptaoxodifosfato(V)] de tetrahierro(II); Pirofosfato (V) de hierro (II);
pirofosfato ferroso
Al2(SO3)3: Tris [trioxosulfato(IV)] de dialuminio; Sulfato (IV) de aluminio; sulfito de aluminio o alumínico
B2) Sales ácidas
Su fórmula general es : Mx (HyNzOw)n Si n=1 no se escribe el paréntesis.
Ejemplos
NaHSO4: hidrógenotetraoxosulfato(VI) de sodio (I); bisulfato o sulfato monoácido de sodio (o sódico)
Fe(HCO3)3: Bis[hidrógenotrioxocarbonato(IV)] de hierro (III); Hidrógeno carbonato (IV) de hierro (III): Bicarbonato férrico
nivelación (video)

































































































No hay comentarios:
Publicar un comentario